Mục lục
- Khởi đầu thời đại phục hồi răng đổi mới: Thử thách của Toregem Biopharma
- Cơ chế hoạt động chính của TRG035: Công nghệ kháng thể trung hòa USAG-1
- Cập nhật tình hình phát triển lâm sàng mới nhất năm 2025 và cột mốc quản lý
- Tài trợ và triển vọng IPO: Thu hút đầu tư chiến lược từ quỹ tài sản nhà nước Nhật Bản
- Kết luận: Sự hấp dẫn đầu tư của Toregem Biopharma và tóm tắt các rủi ro chính
- Câu hỏi thường gặp (FAQ)
Khởi đầu thời đại phục hồi răng đổi mới: Thử thách của Toregem Biopharma
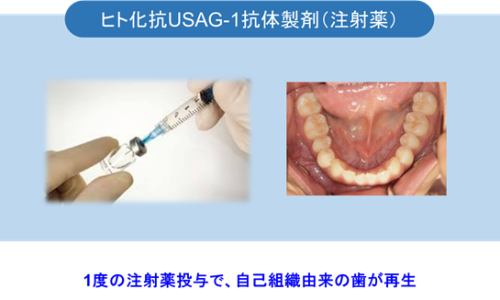
Nha khoa nhân loại từ lâu đã phụ thuộc vào công nghệ phục hồi để thay thế những chiếc răng bị mất bằng các vật liệu nhân tạo. Từ thời cổ đại cho đến hiện nay với các implant titanium, phương pháp thay thế cơ khí đã trở thành tiêu chuẩn.
Nhưng Toregem Biopharma, được thành lập dựa trên các nghiên cứu của Đại học Kyoto vào năm 2020, đang cố gắng thay đổi hoàn toàn cách tiếp cận này bằng một giải pháp sinh học. Công ty đang nỗ lực phát triển công nghệ đổi mới để phục hồi răng và dự kiến sẽ đưa ra một bước ngoặt mới cho nha khoa trong tương lai.

Toregem Biopharma đã phát triển thuốc kháng thể TRG035 đầu tiên trên thế giới có khả năng tái tạo răng người. Thuốc này sẽ vào giai đoạn lâm sàng vào năm 2024 và được kỳ vọng sẽ tạo ra một bước ngoặt đổi mới trong lĩnh vực y học tái sinh.

Vào đầu năm 2024, tôi đã viết về thuốc ung thư giả USAG-1 của Toregem Biopharma. Sau đó, tôi muốn xem xét sâu hơn về độ tin cậy công nghệ, tiến độ lâm sàng, việc thu hút đầu tư chủ yếu và triển vọng IPO của công ty dựa trên dữ liệu mới nhất. Nhờ sự phát triển của công nghệ AI gần đây, việc thu thập thông tin liên quan như tài liệu và bài báo kết quả lâm sàng trở nên dễ dàng hơn nhiều. Tôi mong rằng các dữ liệu này sẽ giúp tôi làm cho bài viết phong phú và đáng tin cậy hơn.

TRG035 định vị bệnh hiếm gặp là bệnh mất răng bẩm sinh làm thị trường khởi đầu. Sau đó, công ty đang thúc đẩy một chiến lược phân khúc nhằm mở rộng sang thị trường rộng lớn hơn là mất răng ở người trưởng thành.
Cơ chế hoạt động chính của TRG035: Công nghệ kháng thể trung hòa USAG-1

Để hiểu giá trị của TRG035, đường ống chính của Toregem Biopharma, cần phải xem xét cơ chế tác động sinh học của nó. Bằng cách nắm rõ các cơ chế này, ta có thể hiểu rõ hơn về hiệu quả và tiềm năng của TRG035.

Thuốc này không tạo ra răng mới, mà hoạt động bằng cách loại bỏ các yếu tố ức chế chương trình phát sinh răng bên trong cơ thể.
Về chức năng của protein USAG-1, quá trình hình thành răng được thúc đẩy bởi protein hình thành xương (BMP) và con đường truyền tín hiệu Wnt. Nhóm nghiên cứu tại Đại học Kyoto đã phát hiện rằng protein USAG-1 (Uterine Sensitization Associated Gene-1) hoạt động như một yếu tố ức chế cản trở các tín hiệu này. Việc kích hoạt USAG-1 dẫn đến việc ngừng hình thành hoặc thoái hóa răng.
Cơ chế hoạt động của TRG035 rất thú vị. TRG035 là một kháng thể đơn dòng nhân hóa (Humanized Monoclonal Antibody) đặc hiệu gắn kết với protein USAG-1 và làm mất hiệu lực chức năng của nó. Khi kháng thể này trung hòa USAG-1, các tín hiệu BMP và Wnt bị ức chế sẽ được kích hoạt lại. Điều này kích thích các mầm răng tiềm năng để quá trình phát sinh có thể được phục hồi.
Ưu điểm của việc phục hồi răng tự nhiên là rất lớn. Phương pháp này cho phép tái tạo răng bằng tế bào của chính bệnh nhân mà không cần cấy ghép vật liệu ngoại lai. Do đó, răng được phục hồi sẽ kết nối với dây thần kinh và mạch máu, và cấu trúc tự thân hoàn hảo với dây chằng nha chu mà không có ở implant. Điều này tạo ra sự khác biệt quan trọng vì răng tự nhiên cung cấp khả năng hấp thụ sốc và chức năng cảm giác. Các kết quả cho thấy rằng “răng thứ ba” đã được hình thành bình thường khi cho kháng thể vào mô hình chuột cát trong giai đoạn tiền lâm sàng.
Nội dung lý thuyết liên quan có thể được xác nhận thêm trong các bài viết trước.
Cập nhật tình hình phát triển lâm sàng mới nhất năm 2025 và cột mốc quản lý

Toregem Biopharma đã đạt được thành tựu phát triển vượt trội khi trở thành một công ty dược sinh học trong giai đoạn lâm sàng từ cuối năm 2024 đến cuối năm 2025.
Vào tháng 9 năm 2024, thử nghiệm lâm sàng giai đoạn 1 đánh giá tính an toàn, khả năng dung nạp và hồ sơ dược động học của TRG035 đã bắt đầu với 30 nam giới khỏe mạnh từ 30 đến 64 tuổi tại Bệnh viện Đại học Kyoto. Thử nghiệm này dự kiến sẽ hoàn thành việc tiêm chính và quan sát vào khoảng tháng 8 năm 2025, và cho đến nay không có báo cáo về tác dụng phụ nghiêm trọng nào, tạo điều kiện cho việc tiến vào giai đoạn 2.
Tình hình tiến triển này nâng cao khả năng phát triển trong tương lai của Toregem Biopharma và có thể tác động tích cực đến quỹ đạo tăng trưởng của công ty. Sự thành công của giai đoạn lâm sàng sắp tới đang trở thành tâm điểm chú ý hơn bao giờ hết.

Kế hoạch thử nghiệm lâm sàng giai đoạn 2 (tập trung vào bệnh nhân nhi):
Thử nghiệm lâm sàng giai đoạn 2 này sẽ tiến hành trên những bệnh nhân nhi từ 2 đến 7 tuổi bị mất răng bẩm sinh hoặc mất hơn 6 chiếc răng. Thời kỳ này là thời kỳ quan trọng khi các vôi răng vĩnh viễn hình thành và sẽ là 'thời điểm vàng' mà đáp ứng với thuốc được dự đoán là mạnh mẽ nhất.
Việc chuẩn bị cho giai đoạn này dự kiến sẽ bắt đầu từ nửa cuối năm 2025, và công tác tuyển chọn và tiêm thuốc cho bệnh nhân sẽ diễn ra vào đầu năm 2026. Sự thành công của giai đoạn này sẽ trở thành một bằng chứng quan trọng cho việc tái tạo răng ở bệnh nhân thực sự. Hy vọng rằng nghiên cứu này sẽ có thể đóng góp cho lĩnh vực phục hồi răng.

Vào ngày 29 tháng 9 năm 2025, Toregem Biopharma đã được Bộ Y tế, Lao động và Phúc lợi Nhật Bản thừa nhận TRG035 là thuốc hiếm dùng để điều trị "mất răng bẩm sinh nghiêm trọng". Sự công nhận này dự báo rằng giá trị của công ty sẽ tăng mạnh.
Hơn nữa, việc chỉ định này mang lại các lợi ích như quyền độc quyền thị trường lên đến 10 năm, rút ngắn thời gian phê duyệt cấp phép thương mại (xét duyệt ưu tiên), giảm thuế cho chi phí nghiên cứu và phát triển, cùng với các hỗ trợ tài chính từ chính phủ. Những yếu tố này dự kiến sẽ ảnh hưởng tích cực đến sự phát triển của công ty trong tương lai.
Tài trợ và triển vọng IPO: Thu hút đầu tư chiến lược từ quỹ tài sản nhà nước Nhật Bản

Toregem Biopharma đã đảm bảo nguồn vốn lớn trong năm 2024 và 2025 để tăng cường tính ổn định tài chính cho sự phát triển lâm sàng thành công.
Vào tháng 8 năm 2024, Toregem đã hoàn thành huy động khoảng 1,5 tỷ yên (khoảng 135 triệu won Hàn Quốc) thông qua việc phát hành cổ phiếu ưu đãi cho bên thứ ba và các khoản trợ cấp từ Cơ quan Nghiên cứu và Phát triển Y tế Nhật Bản (AMED). Đây là một nguồn vốn quan trọng giúp xác định rõ khả năng tăng trưởng trong tương lai của công ty.
Nhà đầu tư chính trong vòng huy động vốn này bao gồm thành viên công ty JIC (Japan Investment Corporation), quỹ tài sản quốc gia do chính phủ Nhật Bản thành lập. Sự tham gia của quỹ quốc gia cho thấy công nghệ của Toregem đã được công nhận như một tài sản chiến lược quốc gia phù hợp với 'Chiến lược sinh học Nhật Bản 2030' của chính phủ. Điều này được dự đoán sẽ cung cấp độ tin cậy cao trong những lần huy động vốn tiếp theo. Ngoài ra, quỹ chuyên dụng của Đại học Kyoto (KYOTO-iCAP) và công ty đổi mới mở gemseki cũng tham gia vào việc cấp vốn này.
Trong số các công ty tham gia đợt huy động vốn này có các công ty niêm yết như Future Venture Capital (đã bị hủy niêm yết và sau đó được niêm yết lại dưới tên AI Fusion Capital Group Corp) và Sanyo Trading (Sanyo Trade), việc giá cổ phiếu của hai công ty này hiện chưa có biến động lớn. Nếu Toregem thúc đẩy IPO, việc đầu tư thông qua mua cổ phiếu trực tiếp sẽ là cách tốt nhất.
Những động thái chiến lược này của Toregem sẽ tạo điều kiện cho sự phát triển bền vững trong lĩnh vực sinh học trong tương lai.

Quản lý rủi ro sản xuất thông qua quan hệ đối tác CDMO:
Toregem đã quyết định hợp tác với Wuxi Biologics, một công ty CDMO hàng đầu thế giới có trụ sở tại Trung Quốc, thay vì xây dựng một nhà máy riêng. Theo thỏa thuận này, việc phát triển dòng tế bào cho TRG035 và sản xuất thử nghiệm GMP sẽ được ủy thác cho bên ngoài.
Chiến lược này sẽ giúp đáp ứng tiêu chuẩn của FDA Hoa Kỳ và EMA châu Âu trong tương lai, đồng thời cung cấp những lợi thế cho quy trình phê duyệt quy định khi thâm nhập thị trường toàn cầu.
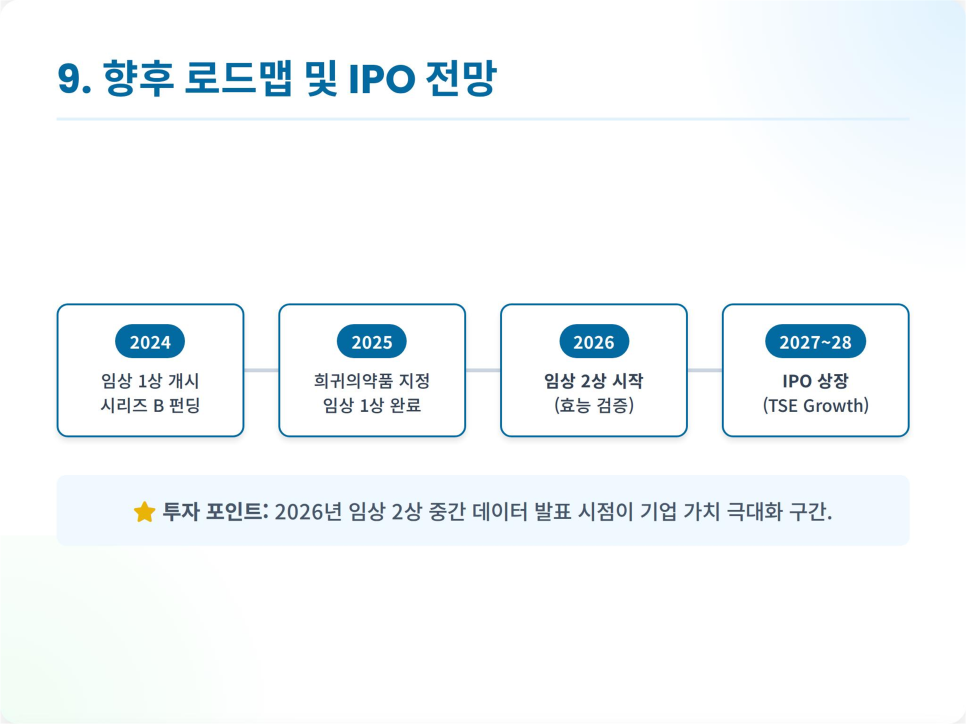
Phân tích triển vọng IPO:
Xét đến tình trạng hiện tại của thử nghiệm lâm sàng, có khả năng cao Toregem Biopharma sẽ được niêm yết trên thị trường tăng trưởng của Tokyo Stock Exchange (TSE) trong giai đoạn lâm sàng 2. Thời gian dự kiến là từ nửa cuối năm 2026 đến nửa đầu năm 2028.
Hơn nữa, việc được lựa chọn vào chương trình J-Startup do Bộ Kinh tế, Thương mại và Công nghiệp Nhật Bản tổ chức vào tháng 3 năm 2025 sẽ cung cấp các điều kiện thuận lợi trong quá trình phê duyệt IPO. Khi dữ liệu giai đoạn 1 được xác định vào cuối năm 2025 và dữ liệu giữa giai đoạn 2 được xác định vào năm 2026, giá trị của công ty được dự đoán sẽ tăng mạnh.
Đặc biệt, chủ đề đổi mới 'tái tạo răng đầu tiên trên thế giới' sẽ thu hút sự chú ý trên thị trường, và có vẻ như tương lai của Toregem Biopharma sẽ rất tươi sáng.
Kết luận: Sự hấp dẫn đầu tư của Toregem Biopharma và tóm tắt các rủi ro chính

Toregem Biopharma đã thành công vượt qua "Thung lũng cái chết (Valley of Death)" trong giai đoạn nghiên cứu cơ bản vào năm 2024 và 2025. Sự tiếp nhận vốn từ các nguồn hỗ trợ chính phủ như JIC, việc gia nhập thử nghiệm lâm sàng giai đoạn 1, và việc được chỉ định trở thành thuốc hiếm mang đến nhiều điều thể hiện rõ năng lực công nghệ và sự phát triển kinh doanh của công ty.
Đặc biệt, TRG035 là một loại thuốc kháng thể đầu tiên có thể gọi là First-in-class, sở hữu công nghệ độc quyền. Sản phẩm này sẽ được phát triển như một thuốc điều trị cho các bệnh hiếm, nhưng trong tương lai có khả năng mở rộng vào thị trường thay thế implant cho người trưởng thành, mang lại sức hút đầu tư mạnh mẽ. Do đó, Toregem Biopharma là một công ty với tiềm năng phát triển rất khả thi trong tương lai.
Khi đầu tư, cần phải lưu ý đến một số yếu tố rủi ro quan trọng. Lưu ý quan trọng nhất là vấn đề an ninh. Tín hiệu BMP/Wnt phân bổ khắp cơ thể, vì vậy trong thử nghiệm lâm sàng giai đoạn 1 cần phải xác minh một cách kỹ lưỡng nguy cơ phát sinh mô xương không mong muốn, tức là xương hóa dị ứng có thể xảy ra ở thận hoặc các cơ quan khác.
Hơn nữa, liệu các sọ răng bị thoái hóa ở người trưởng thành có thể phản ứng với các kích thích của thuốc hay không là yếu tố then chốt trong việc gia nhập thị trường người trưởng thành. Nếu không thành công trong thị trường người trưởng thành, giá trị của công ty có thể bị giới hạn ở mức giá trị thuốc điều trị bệnh hiếm. Điều quan trọng là phải hiểu biết rủi ro này và lập kế hoạch ứng phó thích hợp trước.
Vào cuối năm 2025 hoặc đầu năm 2026, nếu dữ liệu thử nghiệm giai đoạn 1 có kết quả tích cực, Toregem Biopharma sẽ có khả năng nổi bật như một công ty không niêm yết quan trọng trong lĩnh vực sinh học Nhật Bản. Do đó, nhà đầu tư nên chú ý theo dõi các thông báo trong tương lai.
#ToregemBiopharma, #TRG035, #phuchinhanh, #thuocphuchinhanh, #thuocdieutrinha, #dautusinhhoc, #duocduong, #yhoctacsin, #sinhhachnhatban, #USAG1, #thuochiem, #OrphanDrugDesignation, #JICVGI, #DaigakuKyoto, #thumailam1, #thumailam2, #trienkhaiIPO, #dautukhongniemyet, #côngnghệphục hồi răng, #dược sinh học, #bệnh mất răng bẩm sinh, #phuchinhsinh hoc, #tín hiệu BMP, #tín hiệu Wnt, #WuxiBiologics, #CDMO, #răng thứ ba, #côngnghệ sinh học, #phân tích đầu tư, #lĩnh vực sinh học
Câu hỏi thường gặp (FAQ)
Q. Cơ chế hoạt động của TRG035 mà Toregem Biopharma phát triển là gì?
TRG035 là một kháng thể trung hòa USAG-1, giải phóng sự ức chế sự phát sinh răng và thúc đẩy tái tạo răng tự nhiên.
TRG035 là một kháng thể đơn dòng nhân hóa, đặc hiệu gắn kết với protein USAG-1, hoạt động như một yếu tố ức chế trong quá trình hình thành răng. Nó tái kích thích các con đường truyền tín hiệu BMP và Wnt, khôi phục lại các chương trình phát sinh răng bên trong cơ thể, cho phép tái tạo răng hoàn hảo mà không cần cấy ghép ngoại lai, khôi phục được chức năng của răng tự nhiên như dây thần kinh, mạch máu và dây chằng nha chu. Đây là một cách tiếp cận đổi mới.
Q. TRG035 hiện đang ở giai đoạn nào của thử nghiệm lâm sàng và kế hoạch tương lai là gì?
Từ tháng 9 năm 2024, thử nghiệm lâm sàng giai đoạn 1 đang diễn ra, trong khi thử nghiệm giai đoạn 2 dành cho bệnh nhân nhi dự kiến sẽ bắt đầu vào nửa cuối năm 2025.
Vào tháng 9 năm 2024, thử nghiệm lâm sàng giai đoạn 1 đánh giá tính an toàn, khả năng dung nạp và dược động học của TRG035 đã bắt đầu tại Bệnh viện ĐH Kyoto với 30 nam giới từ 30 đến 64 tuổi. Đến tháng 8 năm 2025, việc tiêm chính và quan sát đã hoàn thành. Do chưa có báo cáo về tác dụng phụ nghiêm trọng nào, việc vào giai đoạn 2 được kỳ vọng cao. Giai đoạn 2 sẽ tập trung vào bệnh nhi bị mất răng bẩm sinh và dự kiến sẽ bắt đầu vào nửa cuối năm 2025, với tuyển chọn và tiêm thuốc bắt đầu vào đầu năm 2026. Giai đoạn này sẽ là một bước quan trọng trong việc chứng minh hiệu quả phục hồi răng.
Q. Ý nghĩa và lợi ích của việc được chỉ định thuốc hiếm mà Toregem Biopharma nhận được là gì?
'Trị liệu cho chứng mất răng bẩm sinh nghiêm trọng' được Bộ Y tế, Lao động và Phúc lợi Nhật Bản công nhận là thuốc hiếm, điều đó có nghĩa là xác nhận quyền độc quyền và các lợi ích thuế.
Vào ngày 29 tháng 9 năm 2025, TRG035 của Toregem Biopharma được Bộ Y tế, Lao động và Phúc lợi Nhật Bản công nhận là thuốc hiếm dùng cho điều trị mất răng bẩm sinh nghiêm trọng. Việc chỉ định này đảm bảo quyền độc quyền thị trường lên đến 10 năm, rút ngắn thời gian xét duyệt cấp phép, thuế ưu đãi cho chi phí nghiên cứu và phát triển và nhận hỗ trợ từ chính phủ. Nhờ các yếu tố này, giá trị của công ty sẽ tăng lên, tạo ra một môi trường thuận lợi cho việc phát triển và thương mại hóa thuốc.
Q. Tình trạng tài trợ hiện tại của Toregem Biopharma và các nhà đầu tư chính là ai?
Đã thực hiện vòng gọi vốn B trị giá khoảng 1,5 tỷ yên vào năm 2024, trong đó có các nhà đầu tư chính là công ty con của quỹ tài sản nhà nước Nhật Bản JIC.
Vào tháng 8 năm 2024, Toregem đã hoàn thành vòng gọi vốn B trị giá khoảng 1,5 tỷ yên (khoảng 135 triệu won Hàn Quốc), bao gồm phát hành cổ phiếu ưu đãi cho bên thứ ba và trợ cấp từ cơ quan nghiên cứu y tế Nhật Bản AMED. Các nhà đầu tư chính bao gồm JIC VGI, một công ty con của quỹ tài sản nhà nước JIC do chính phủ Nhật Bản thành lập, cho thấy công nghệ và các hoạt động của Toregem phù hợp với chiến lược sinh học quốc gia Nhật Bản 2030. Quỹ chuyên dụng của Đại học Kyoto (KYOTO-iCAP), Gemseki, cùng các công ty niêm yết Future Venture Capital và Sanyo Trading cũng tham gia.
Q. Dự đoán về IPO của Toregem Biopharma và thời gian dự kiến niêm yết là khi nào?
Có khả năng cao công ty sẽ niêm yết trên thị trường tăng trưởng của sàn giao dịch chứng khoán Tokyo (TSE) từ giai đoạn lâm sàng 2 vào khoảng giữa năm 2026 đến giữa năm 2028.
Xét theo tình hình hiện tại của các thử nghiệm lâm sàng, Toregem Biopharma có lẽ sẽ niêm yết trên thị trường tăng trưởng của TSE trong giai đoạn lâm sàng 2, dự kiến từ giữa năm 2026 đến giữa năm 2028. Việc được lựa chọn vào chương trình J-Startup do Bộ Kinh tế, Thương mại và Công nghiệp Nhật Bản tổ chức vào tháng 3 năm 2025 có thể cung cấp sự thuận lợi trong quá trình phê duyệt niêm yết. Dự kiến, giá trị công ty sẽ tăng mạnh khi có dữ liệu của giai đoạn 1 vào cuối năm 2025 và dữ liệu trung gian của giai đoạn 2 vào năm 2026, trong khi chủ đề hấp dẫn về 'thuốc tái tạo răng đầu tiên trên thế giới' có thể thu hút sự chú ý của các nhà đầu tư.
Q. Các nguy cơ chính cần lưu ý khi đầu tư vào Toregem Biopharma là gì?
Rủi ro liên quan đến vấn đề an toàn và khả năng thâm nhập vào thị trường người trưởng thành là mối quan tâm lớn; cần chú ý đến tác dụng phụ và phản ứng tái tạo răng ở người trưởng thành.
Vì tín hiệu BMP/Wnt ảnh hưởng đến nhiều mô trong cơ thể, nên trong giai đoạn 1 cần phải xác minh những nguy cơ có thể xảy ra như sự hình thành xương không mong muốn có thể xảy ra trong thận và các cơ quan khác. Hơn nữa, liệu các tế bào răng bị thoái hóa ở người trưởng thành có thể phản ứng với thuốc hay không là vấn đề then chốt trong việc thâm nhập thị trường người trưởng thành. Nếu không thành công trong thị trường người trưởng thành, giá trị của công ty có nguy cơ bị hạn chế ở mức giá trị thuốc hiếm. Do đó, việc nắm bắt các yếu tố rủi ro liên quan đến an toàn và hiệu quả là cần thiết để xây dựng các chiến lược ứng phó.