目录
创新牙齿再生时代的序幕:托瑞金生物制药的挑战
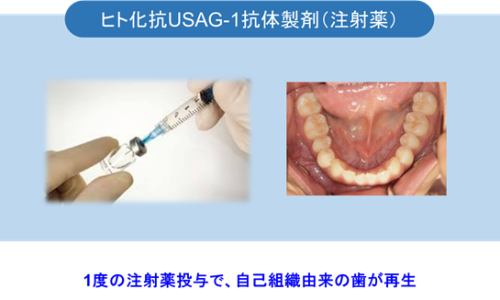
人类的牙医学长期以来依赖于用人工物来替代失去的牙齿的修复技术。从古代的修复方式到如今的钛合金植入物,机械替代方式已成为标准。
但自2020年成立的托瑞金生物制药(Toregem Biopharma)基于京都大学的研究成果,正在尝试采用全新的生物学方法彻底打破这一传统框架。该公司致力于开发用于牙齿再生的创新技术,预计将为未来牙医学带来新的转折点。

托瑞金生物制药首次开发了能够使人类牙齿再生的单克隆抗体药物TRG035。该药物将在2024年进入临床阶段,预计将为再生牙医学领域带来创新转折点。

在2024年初,我撰写了关于托瑞金生物制药的USAG-1基因蛋白抑制药物的文章。之后,我将基于最新的数据深入分析该公司的技术可信度、临床进展、主要投资吸引及未来IPO前景等问题。得益于最近人工智能技术的进步,收集相关信息或临床结果论文等资料变得更为轻松。通过这些资料,我希望能提供更丰富和可信的发布内容。

TRG035设定了先天性无齿症作为初期市场。之后,该公司还采取了双重战略,旨在扩大至成年人牙齿缺失这一大规模市场。
TRG035的关键作用机制:USAG-1中和抗体技术

为了准确理解托瑞金生物制药主要管线TRG035的价值,必须观察该物质的分子生物学作用机制。通过了解这些机制,可以更清晰地认识到TRG035的效果和潜力。

该药物的工作原理并不是产生新的牙齿,而是通过消除体内潜在的牙齿发生程序抑制因子来发挥作用。
关于USAG-1蛋白的功能,牙齿形成过程是由骨形成蛋白(BMP)和Wnt信号通路所促进。京都大学的研究小组已经揭示,USAG-1(子宫敏感性相关基因1)蛋白作为这种信号传导的抑制因子发挥作用。USAG-1的激活会导致牙齿形成的中断或退化。
TRG035的作用机制非常有趣。TRG035是一种特异性结合USAG-1蛋白并使其功能失效的人源单克隆抗体(Humanized Monoclonal Antibody)。当这种抗体中和USAG-1时,受到抑制的BMP和Wnt信号会重新被激活。因此,潜在的牙齿萌芽会受到刺激,发育过程得以重新开始。
天然牙齿再生的优势非常明显。这种方法能够不移植外部物质而利用患者自身的细胞进行牙齿再生。因此,再生的牙齿与神经和血管相连,并具有植入体中无法找到的牙周韧带(Periodontal Ligament),形成完美的自体组织。这成为提供天然牙齿的冲击吸收能力和感应功能的重要差异点。在前临床阶段,当给费勒模型单次注射抗体时“第三颗牙”正常形成的结果也被确认。
有关此内容的理论材料可通过之前的发布进一步确认。
2025年最新临床开发现状和监管里程碑

托瑞金生物制药在2024年下半年至2025年末取得了成长为临床阶段生物制药公司的成果。
2024年9月,在日本京都大学附属医院对30名年龄在30岁至64岁之间的健康男性开展了评估TRG035的安全性、耐受性和药代动力学特征的I期临床试验。此次临床试验预计将在2025年8月完成主要给药和观察,至今未报告严重副作用,预计可以进入II期临床。
这一进展提高了托瑞金生物制药未来发展的潜力,并可能对此公司成长轨迹产生积极影响。接下来的临床阶段的成功与否更加引人注目。

II期临床试验计划(以儿童患者为中心):
此次II期临床试验将针对2至7岁间患有先天性无齿症或缺失6颗以上的严重部分无齿症的儿童进行。此时恰逢恒牙胚开始形成的重要时期,预计将是药物反应最为活跃的“黄金时间”。
预计在2025年下半年正式开展准备工作,并在2026年初进行患者招募和给药。此阶段的成功与否将成为验证真实患者牙齿再生的重要证明。希望此次研究能够为牙齿再生领域做出贡献。

2025年9月29日,托瑞金生物制药的TRG035被日本厚生劳动省认可为“严重先天性无齿症”治疗的稀有药物。这样的指定预计将大幅提升公司的价值。
此外,该指定还提供最多10年的市场独占权保障,并享有审评周期的缩短(优先审查)、研发费用的税收减免以及政府的补助等多项战略性福利。这些因素预计将积极影响公司的未来增长。
融资及IPO前景:日本国富基金的战略投资吸引

托瑞金生物制药在2024年和2025年之间成功获得了大规模资金,以进一步增强临床开发的财务稳定性。
2024年8月,托瑞金通过第三方指定增资和日本医疗研发机构AMED的补助成功完成约150亿日元(约合135亿韩元)规模的B轮融资。这为公司的未来增长奠定了坚实的资金基础。
此次投资轮的主要投资者为日本政府成立的国富基金JIC(Japan Investment Corporation)的子公司JIC创业成长投资(JIC VGI)。国富基金的参与表明托瑞金的技术被认定为符合日本政府的“2030生物战略”的国家战略资产。这预示着今后若进行进一步融资将获得高可信度。同时,京都大学专用基金(KYOTO-iCAP)和开放创新专业企业Gemseki也参与了此次融资。
本次融资参与的企业中,包括上市公司Future Venture Capital(在退市后以AI Fusion Capital Group Corp重新上市)和三阳贸易(Sanyo Trading),而这两家公司的股价目前并未大幅波动。如果托瑞金推进IPO,直接购买股份将是最佳投资方式。
托瑞金的这一战略举动将成为未来在生物领域持续增长的重要因素。

通过CDMO伙伴关系来管理制造风险:
托瑞金决定与全球领先的CDMO公司吴市生物制药合作,而不是自行建厂。根据协议,将把TRG035的细胞株开发和临床样品的GMP生产外包给吴市生物制药。
这一策略将有助于满足未来美国FDA和欧洲EMA的标准,为全球市场的监管审批程序铺平道路。
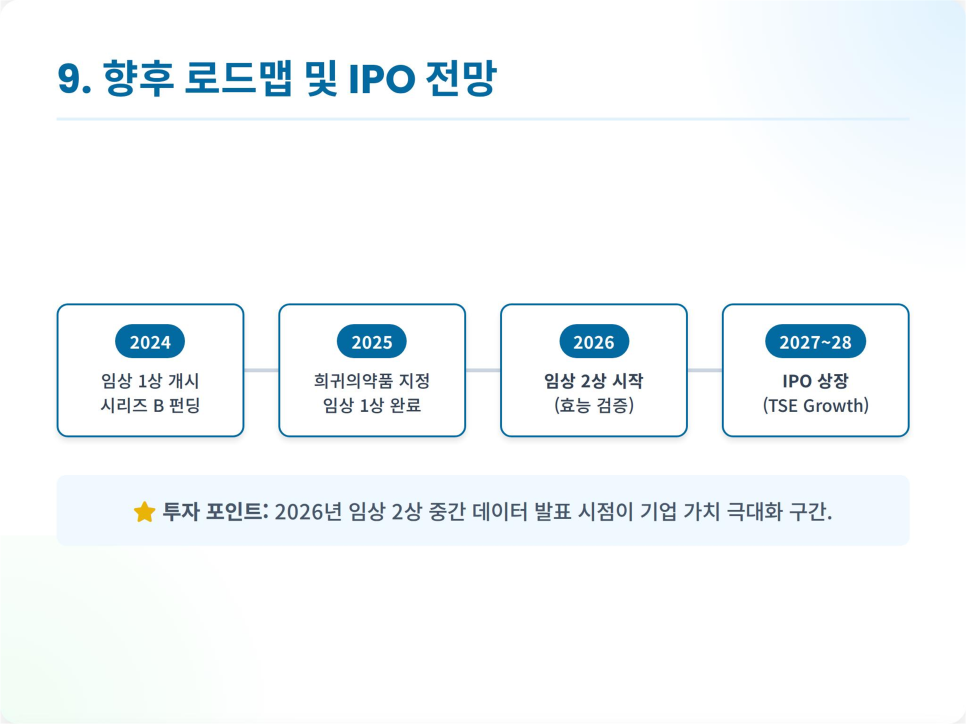
对IPO前景的分析:
在当前临床进展的情况下,托瑞金生物制药可能在临床II期阶段于东京证券交易所(TSE)成长市场上市。预计的时间为2026年下半年至2028年上半年。
此外,通过在2025年3月日本经济产业省主办的J-Startup计划中入选,有望在IPO审查过程中获得有利条件。到2025年底,I期数据将得到确认,2026年将产生II期中期数据,预计公司价值将大幅上升。
尤其是“世界首个牙齿再生”的创新主题,将在市场上受到关注,这也将使得托瑞金生物制药的未来非常光明。
结论:托瑞金生物制药的投资吸引力及核心风险总结

托瑞金生物制药在2024年和2025年期间成功跨越了基础研究阶段遇到的“死亡谷(Valley of Death)”。政府资助资金的输入,如JIC,I期临床试验的推进,以及被指定为稀有药物的事实,均很好地表明了该公司的技术实力和商业成长。
尤其是TRG035作为没有竞争者的首创药物,拥有独特的技术实力。虽然该产品最初是作为稀有病治疗药物开发的,但未来希望通过向成年人植入替代市场的扩展,保持强劲的投资吸引力。因此,托瑞金生物制药的未来增长潜力备受期待。
投资时必须考虑一些重要风险因素。首先要考虑的是安全性问题。由于BMP/Wnt信号在体内的多个部位分布,因此在I期临床试验中必须详细验证可能出现在肾脏或其他器官的非预期骨生长,即异位骨化的副作用。
此外,与动物模型不同,成人的退化牙板是否会对药物刺激做出反应,成为进入成人市场的关键因素。如果在成人市场中失败,公司的价值可能会被限制在稀有病治疗药物的水平。因此,提前识别这些风险,制定应对战略显得至关重要。
如果2025年底或2026年初发布的I期数据是积极的,托瑞金生物制药有望成为日本生物领域的重要非上市公司。因此,投资者应仔细关注未来的公告。
#托瑞金生物制药, #TRG035, #牙齿再生, #牙齿再生新药, #牙科治疗药物, #生物投资, #生物制药, #再生医学, #日本生物, #USAG1, #稀有药物, #OrphanDrugDesignation, #JICVGI, #京都大学, #临床1期, #临床2期, #IPO前景, #非上市投资, #牙齿再生技术, #生物制药, #先天性无齿症, #生物学牙齿再生, #BMP信号, #Wnt信号, #吴市生物制药, #CDMO, #第三颗牙, #生物技术, #投资分析, #生物部门
常见问题(FAQ)
Q. 托瑞金生物制药开发的TRG035的作用机制是什么?
TRG035是通过中和USAG-1蛋白,解除牙齿发生抑制并促进自然牙齿再生的抗体。
TRG035是一种人源单克隆抗体,特异性结合在牙齿形成过程中作用为抑制子的USAG-1蛋白,使其功能失效。通过重新激活USAG-1抑制的BMP和Wnt信号传导通路,可以重新启动内在的牙齿发生程序,从而实现自然牙齿再生。这项技术无需外部移植,能够完美地利用自身细胞再生牙齿,并恢复自然牙齿的神经、血管、牙周韧带等功能,是一种创新的方法。
Q. TRG035临床试验目前处于哪个阶段,未来计划如何?
自2024年9月以来进入I期临床试验,并计划于2025年下半年开展以儿童患者为对象的II期临床试验。
2024年9月,在京都大学附属医院对30名年龄在30至64岁的男性开展了评估TRG035的安全性、耐受性和药代动力学的I期临床试验,该研究预计于2025年8月完成主要给药和观察。截至目前未报告严重副作用,预计即将进入II期临床。II期将以先天性无齿症等儿童患者为对象,预计将在2025年下半年开始准备,并于2026年初进行患者招募和给药。成功后将成为验证牙齿再生效果的重要阶段。
Q. 托瑞金生物制药获得稀有药物指定的意义和好处是什么?
作为“严重先天性无齿症”的治疗药物,获得日本厚生劳动省的稀有药物指定,确保市场独占权和税收优惠等多项福利。
2025年9月29日,托瑞金生物制药的TRG035被日本厚生劳动省指定为“严重先天性无齿症”治疗的稀有药物。该指定提供最多10年的市场独占权保障、简化审批流程(优先审查)、研发费用的税收减免和政府补助等多项国家层面的好处。通过这些措施,公司的价值将提高,有利于治疗药物的开发和商业化,预计将积极影响公司成长。
Q. 托瑞金生物制药的资金筹集状况和主要投资者有哪些?
成功融资约150亿日元的B轮项目,主要投资者为日本国富基金JIC的子公司等。
2024年8月,托瑞金通过第三方指定增资和日本医疗研究开发机构AMED的补助完成了约150亿日元(约合135亿韩元)的B轮融资。主要投资者是日本政府成立的国富基金JIC的创业投资子公司JIC VGI,这意味着托瑞金的技术与项目吻合日本国家生物战略2030。京都大学专用基金(KYOTO-iCAP)、Gemseki、上市公司Future Venture Capital和三阳贸易等也参与了投资。
Q. 托瑞金生物制药的未来IPO前景如何,预计上市时间是?
预计在2026年下半年至2028年上半年,进入东京证券交易所成长市场上市。
根据当前临床进展,托瑞金生物制药在2026年下半年至2028年上半年进入东京证券交易所(TSE)成长市场上市的可能性很高。通过在2025年3月获得日本经济产业省主办的J-Startup计划的立项,有望为上市审查过程提供便利。特别是如果在2025年底获得I期数据,并在2026年获得II期中期数据,将使得公司的价值大幅上升,并期待以“世界首个牙齿再生药物”的主题引起投资者的关注。
Q. 托瑞金生物制药投资时需考虑的主要风险是什么?
安全性验证和成人市场进入可能性是核心风险,需要关注副作用和成人牙齿再生反应。
由于BMP/Wnt信号在体内多个组织的影响,在I期临床试验中,必须详细验证在肾脏等可能发生的副作用——异位骨化。因此,成人的退化齿槽内的牙板对药物动能的反应是否存在,也成为进入成人市场扩展的关键。如果在成人市场失败,企业价值可能会停留在稀有疾病治疗级别。因此,提前识别这些安全性和效果相关的风险,并制定应对战略显得特别重要。